Les piles et les réactions d'oxydoréduction/Les piles
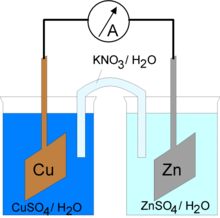
Une pile permet de transformer l'énergie chimique en énergie électrique grâce à une réaction redox. En effet, les électrons transférés lors de cette réaction passent par un circuit extérieur afin de l’alimenter.
L'électrode est la partie métallique de la pile où sa branche est le circuit extérieur. Si à l'électrode on a une oxydation, on parle d'anode. Si à l'électrode on a une réduction, on dit que c'est une cathode.
On peut déterminer le sens des électrons dans le circuit extérieur grâce aux demi-équations. Ce qui permet ensuite de déterminer l'électrode positive et l'électrode négative de la pile car les électrons vont de la pile négative vers la pile positive. On peut ensuite déterminer le sens du courant car celui-ci va toujours de la pile positive vers la pile négative.
Le pont salin est mis à la fonction des deux béchers afin que sa pile puisse fonctionner. Par sa présence et par les cations et anions qu'il contient, il permet :
- de former le circuit électrique
- maintenir les solutions électriquement neutres


