Introduction à la science des matériaux/Annexe/Étude du tableau périodique
Différentes parties du tableau
[modifier | modifier le wikicode]

La plupart des éléments se trouvent naturellement dans la nature. Certains éléments sont artificiels : ils se désintègrent rapidement, de ce fait, les atomes qui existaient lors de la création de la Terre ont déjà tous disparus. Parmi les éléments artificiels, on a :
- les produits de désintégration : des atomes d'éléments naturels, en se désintégrant, produisent des atomes de ces éléments, et ces atomes eux-même se désintègrent par la suite ;
- les éléments synthétiques : on n'en a jamais observé dans la nature, ils ont été produits dans des accélérateurs de particules.
Notons que le neptunium (Np, Z = 93) et le plutonium (Pu, Z = 94) que l’on trouve dans la nature proviennent de la désintégration naturelle des minerais d'uranium ; les atomes qui pouvaient être présent lors de la création de la Terre ont eux disparu.
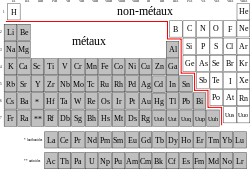
On distingue deux grandes catégories d'éléments : les métaux et les non-métaux. La séparation est une ligne diagonale allant du bore au polonium. L'hydrogène, aux très fortes pressions, cristallise et forme un métal, mais ce phénomène n'ayant pas lieu dans les conditions habituelles sur Terre, il n'est habituellement pas considéré comme un métal.

Parmi les non-métaux, certains éléments sont regroupés dans des familles :
- les métalloïdes, ce sont les éléments les plus proches des métaux ;
- les halogènes, ils constituent l'avant-dernière colonne du tableau ;
- les gaz rares, ou gaz nobles, encore appelés gaz inertes, qui constituent la dernière colonne.
Ce pense-bête marche pour tous les gaz nobles à l'exception de l'hélium.
Noble commence par N O et les noms des gaz nobles (à l'exception de l'hélium) se terminent par O N (c'est l'inverse) :
- Néon,
- Argon,
- Krypton,
- Xénon,
- Radon,
- Oganesson.
Aucun autre élément ne se termine en -on. Comme ils se terminent par O N, ils terminent le tableau, et sont donc tout à droite. Cette astuce permet de se rappeler :
- que les gaz nobles sont dans la dernière colonne,
- qu'un élément est un gaz noble ou pas,
- la liste des gaz nobles.
Attention, cette astuce marche en français, pas en anglais par exemple.

Parmi les métaux, on dénombre :
- les métaux de transition, ils forment le cœur du tableau ;
- les alcalins, qui constituent la première colonne ;
- les alcalino-terreux, qui forment la deuxième colonne ;
- les métaux pauvres, qui forment la droite du tableau ;
- les lanthanides, dont la ligne est en général déportée sous le tableau ;
- et les actinides, dont la ligne est également déportée, qui comportent en particulier des métaux radioactifs comme l'uranium (U, Z = 92) et le plutonium (Pu, Z = 94) ; les « transuraniens » sont les actinides « plus lourds » que l'uranium (Z > 92), ce sont en particulier les déchets radioactifs des centrales nucléaires : plutonium (Pu, Z = 94), américium (Am, Z = 95), curium (Cm, Z = 96).

Enfin, la famille des terres rares regroupe l'yttrium, le scandium (donc la 3e colonne) et les lanthanides.
Remplissage des couches électroniques
[modifier | modifier le wikicode]- Règle générale
- Dans le tableau de classification périodique, tous les éléments d'une même colonne ont le même nombre d'électrons sur leur couche périphérique
Cette dernière règle est bien respectée pour les quatre colonnes de gauche et les six colonnes de droite ; dans les colonnes centrales, la dernière couche contient 1 ou 2 électrons (sauf pour le palladium qui en contient 18).
| Colonne | IA | VIIIA | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| IIA | IIIA | IVA | VA | VIA | VIIA | |||||||||||||
| IIIB | IVB | VB | VIB | VIIB | VIIIB | IB | IIB | |||||||||||
| Couche externe | 1 | 2 | 2 | 2 | 2/1 | 2/1 | 2/1 | 2/1 | 2/1 | 2/1/18 | 2/1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
Voir la table avec le remplissage des niveaux.
Valence
[modifier | modifier le wikicode]| Colonne | IA | VIIIA | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| IIA | IIIA | IVA | VA | VIA | VIIA | |||||||||||||
| IIIB | IVB | VB | VIB | VIIB | VIIIB | IB | IIB | |||||||||||
| Nb d'e- dans la couche externe | 1 | 2 | 2 | 2 | 2/1 | 2/1 | 2/1 | 2/1 | 2/1 | 2/1/18 | 2/1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| Valence | 1 | 2 | 3 | 4 | 5 | 6 | 4/6/7 | 2/3/5/7 | 2/4/6 | 3/5 | 4 | 3/5 | 2/6 | 1/5/7 | 0 | |||
Voir la table des valences.
Charge des ions
[modifier | modifier le wikicode]| Colonne | IA | VIIIA | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| IIA | IIIA | IVA | VA | VIA | VIIA | |||||||||||||
| IIIB | IVB | VB | VIB | VIIB | VIIIB | IB | IIB | |||||||||||
| Nb d'e- dans la couche externe | 1 | 2 | 2 | 2 | 2/1 | 2/1 | 2/1 | 2/1 | 2/1 | 2/1/18 | 2/1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| Charge des ions | + | 2+ | 3+ | 3+/4+ | 3+/4+/5+ | 2+/3+/6+ | 2+/4+/7+ | 2+/3+/4+ | +/2+/3+ | +/2+ | 0/+/3+ | 0/2+/4+ | 3-/4+/5+ | 2-/2+/4+ | - | 0 | ||



