Introduction à la cristallographie/Systèmes cristallins
La matière solide se caractérise par une cohésion relativement forte : un corps solide, bien qu'éventuellement déformable, n'occupera pas tout l'espace d'une pièce (comme le ferait un gaz) ni ne prendra la forme de son contenant (comme le ferait un liquide). À quelques exceptions près, il s'agit également de l'état de la matière la plus dense[1]. Cela s'explique par l’existence d'interactions entre ses composants (atomes, ions, molécules…), de nature attractive. Selon la nature exacte de ces composants, ces interactions seront de différente nature (liaisons hydrogène, forces de Van der Waals…).
Ainsi contrainte à occuper un minimum d'espace, la matière adopte souvent des configurations régulières : ce sont les cristaux. Les matériaux solides mais irréguliers sont, généralement, appelés « matériaux amorphes ».
Le cristal « parfait »
[modifier | modifier le wikicode]Le modèle de base pour étudier un cristal est de pousser ses propriétés à l'extrême :
Un cristal parfait est un empilement ordonné, infini, d'atomes (d'ions, de molécules…) identiques.
Dans beaucoup de cas, cet ordre se caractérise par :
- une périodicité[2] : le motif cristallin se répète dans l'espace ;
- des symétries : plans, axes ou centres de symétries.
Le cristal parfait n'existe pas, mais peut constituer un modèle valable sur des échelles telles que les dimensions du cristal sont très petites devant la zone observée.
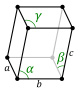
La maille élémentaire ou primitive est la plus petite unité de répetition par translation du cristal : elle est répétée par translation, identique à elle-même, dans tout le solide. Elle est caractérisée par la donnée de trois vecteurs : a, b, c et trois angles interaxiaux, α (entre b et c), β (entre a et c) et γ (entre a et b). D'autres mailles, plus grandes, peuvent aussi être utilisées pour décrire le même cristal : elles sont dites mailles centrées car elles contiennent des nœuds du réseau au centre des faces ou du volume.
La structure cristalline est la répétition périodique et régulière du contenu de la maille. Cette répétition est quand même affectée par différents types de défauts. Le cristal parfait est obtenu en négligeant ces défauts et en prolongeant à l'infini la répétition de la maille : on parle alors de motif cristallin, qui est l'idéalisation de la structure cristalline.
Notion de périodicité dans un cristal : les systèmes réticulaires
[modifier | modifier le wikicode]La classification des cristaux sur la base de la symétrie de translation donne lieu à sept systèmes réticulaires. La maille élémentaire est délimitée par un ensemble de points, appelés nœuds ; l’ensemble des nœuds constitue un réseau cristallin (réseau de Bravais).
On peut alors classer tout agencement cristallin dans l'une des sept catégories, dites « systèmes réticulaires », en fonction des propriétés de symétrie du réseau de Bravais :
- triclinique ;
- monoclinique ;
- orthorhombique ;
- tétragonal ;
- rhomboédrique ;
- hexagonale ;
- cubique.
Classification morphologique des cristaux : les systèmes cristallins
[modifier | modifier le wikicode]La classification des cristaux sur la base de leur symétrie morphologique, ainsi que de la symétrie de leurs propriétés physiques, fut introduite par les cristallographes allemands sous le nom de système cristallin, qui a été retenu comme nom officiel par l'Union internationale de cristallographie.
Un système cristallin regroupe tout cristal caractérisé par la présence d'éléments de symétrie minimaux, auxquels peuvent éventuellement s'en ajouter d'autres jusqu'à obtenir la symétrie d'un réseau. Un cristal qui possède la pleine symétrie de son réseau est dit holoèdre ; un cristal dont la symétrie est inférieure à celle de son réseau est dit mérièdre. La combinaison de ces éléments de symétrie donne lieu à sept « systèmes cristallins » :
- triclinique ;
- monoclinique ;
- orthorhombique ;
- tétragonal ;
- trigonal ;
- hexagonale ;
- cubique.
Trigonal versus rhomboédrique
[modifier | modifier le wikicode]Dans le milieu minéralogique francophone, les deux adjectifs, trigonal et rhomboédrique, sont souvent considérés comme équivalents. Pourtant le terme trigonal qualifie tout cristal ayant comme symétrie rotationnelle d'ordre maximal une rotation de ±120º autour d'un seul axe, indépendamment du type de réseau (hexagonal ou rhomboédrique) : il caractérise donc un système cristallin et non un réseau. En revanche, le terme rhomboédrique qualifie tout cristal ayant un réseau de symétrie m : il caractérise cette fois un système réticulaire et non un système cristallin. La cause de cette confusion dans la littérature minéralogique est que primitivement les deux types de système étaient qualifiés de "cristallin".
Réseaux de Bravais
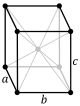
[modifier | modifier le wikicode]La symétrie du réseau est parfois mieux mise en évidence en utilisant, au lieu d'une maille élémentaire (primitive), une maille centrée, de plus grand volume. Les différentes mailles alors envisageables, au nombre de 14, constituent les 14 réseaux de Bravais. Les voici toutes :
Concernant cette introduction, nous nous intéresserons en particulier aux systèmes cubiques et hexagonaux. On peut remarquer qu’à chaque maille ci-dessus (appelées mailles conventionnelles) est associé un code de deux lettres — il s'agit d'une convention permettant d’identifier rapidement la structure d'un cristal dans un catalogue.
On peut, enfin, remarquer les « vides » à l'intérieur de ces mailles. Si cela s'explique aisément par les arguments développés au chapitre suivant (si les atomes ne se repoussaient pas, la matière s'effondrerait…), nous verrons également que ces espaces vides sont parfois occupés !
Paramètres supplémentaires
[modifier | modifier le wikicode]Étant donné un certain système cristallin, on peut en déduire certaines informations qui ont des répercussions sur des propriétés physiques macroscopiques. En particulier, nous nous attacherons à :
- la population d'une maille, c'est-à-dire le nombre d'atomes (d'ions, de molécules…) contenus dans une maille ;
- la coordinence d'un atome (ion, molécule…), c'est-à-dire le nombre de ses plus proches voisins dans le cristal ;
- la compacité d'un cristal (qui sera plus aisément définie dans le chapitre suivant), c'est-à-dire le rapport du volume des atomes d'une maille par le volume de la maille ;
- la masse volumique d'un cristal, c'est-à-dire le rapport de la masse d'une maille sur son volume.
Incidemment, nous devrons préciser à nouveau la définition de la coordinence pour des assemblages ioniques, et donner un sens précis à la compacité — ce que nous ferons dans le chapitre suivant. La population, la coordinence et la compacité d'une maille sont caractéristiques de celle-ci.
Différents types de solides
[modifier | modifier le wikicode]On peut définir encore quelques notions :
- Solide monocristallin : solide obtenu par répétition périodique d'une maille, à quelques défauts ponctuels éventuels près ;
- Solide polycristallin : solide obtenu par juxtaposition aléatoire de monocristaux ;
- Solide amorphe : solide ne présentant pas de structure particulière ;
- Cristal liquide : liquide présentant un ordre à longue distance (fortement anisotrope) — ce n’est pas un cristal.
Remarques
[modifier | modifier le wikicode]- ↑ Les quelques exceptions étant, pour l'essentiel, l'eau, le gallium, le silicium, le germanium et le bismuth. Le fait que ces composés soient moins denses que leurs liquides s'explique, comme nous le verrons, grâce à la cristallographie.
- ↑ Il existe des solides, appelés « quasi-cristaux », qui sont réguliers mais remarquables par leur absence de périodicité dans l'espace tridimensionnel. Nous ne les abordons pas ici.