Propriétés des gaz/Description du gaz
Apparence
Description microscopique
[modifier | modifier le wikicode]- v ≈ 500 m s−1
Description macroscopique
[modifier | modifier le wikicode]À une température ambiante, 1 litre de gaz contient de l’ordre de 1022 molécules. Il est donc impossible de connaître le mouvement de chaque molécule prise séparément. On fait appel à des grandeurs macroscopiques. On décrit un gaz à l’aide de 4 variables :
- la pression
- le volume
- la température
- la quantité de matière, en moles
Les variables extensives
[modifier | modifier le wikicode]Les variables extensives sont des variables qui s’additionnent, par exemple le volume et la quantité de matière.
Les variables intensives
[modifier | modifier le wikicode]Les variables intensives sont des variables qui ne s’additionnent pas, par exemple la température et la pression.
-
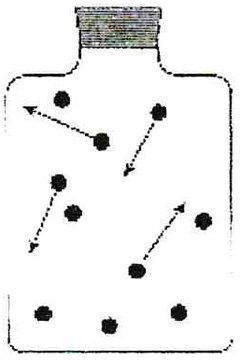
Un gaz est constitué de molécules éloignées les unes des autres par rapport à leurs dimensions.
-
Les molécules sont en mouvement continuel. Ce mouvement s'effectue en ligne droite.
-
Les molécules rebondissent sur les parois du récipient. Leur trajectoire est alors modifiée.
-
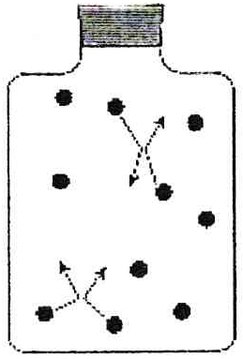
Deux molécules peuvent rentrer en collision. Elles changent alors toutes les deux de direction.
-
Le manomètre métallique est constitué d'un tube creux qui se déforme sous l'action des forces pressantes.