Glucide : Principaux oses
Glucide/Principaux oses
Importance des oses
[modifier | modifier le wikicode]Présentation générale des oses
[modifier | modifier le wikicode]L'ose est le composé de base de l’ensemble des glucides. La molécule chimique d’un ose contient :
- un ou plusieurs groupements alcool :
- ainsi que :
- un groupement aldéhyde (on parle alors d'aldose):
- ou bien un groupement cétone (on parle alors de cétose):
La fonction obtenue dans la molécule étant alors celle de l'ose.
Il existe plusieurs classifications des oses :
- selon la fonction que la molécule porte (aldéhyde ou cétone)
- selon le nombre de carbones (3 carbones pour un triose, 5 pour un pentose ou 6 pour un hexose par exemple)
- selon le caractère structural de la molécule : de série D ou L du carbone asymétrique d’après la projection de Fisher
- selon le pouvoir rotatoire de la molécule : dextrogyre quand la lumière polarisée est déviée à droite, lévogyre quand elle l'est à gauche.
| Ne pas confondre série D/L et caractère dextrogyre/levogyre, ils n'ont rien en commun ! |
Quelques exemples :
- le glycéraldéhyde (triose à groupement aldéhyde)
Cette molécule est le plus souvent présente sous forme phosphorylée pour une utilisation énergétique dans le cycle de Calvin de la photosynthèse (on parle alors de G3P pour glycéraldéhyde 3 phosphate):
- le dihydroxyacétone (triose à groupement cétone)
- le ribose (pentose à groupement aldéhyde)
Le ribose est le précurseur des acides nucléiques. Sur cette molécule le quatrième C en partant du haut possède une fonction OH à droite : c’est une molécule de D-ribose.
- le ribulose (pentose à groupement cétone)
Par un même raisonnement, on observe que cette molécule est un D-ribulose. Par ailleurs, cette molécule est le plus souvent présente sous forme phosphorylée pour une utilisation énergétique dans le cycle de Calvin de la photosynthès (on parle alors de D-ribulose-1,5bisP) :
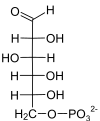
- le glucose (hexose à groupement aldéhyde)
Cette molécule est un D-glucose.
Le glucose est une molécule capitale dans le métabolisme : elle est le précurseur de nombreuses synthèses. Sa dégradation par la respiration cellulaire (glycolyse puis cycle de Krebs) fournit de l'énergie immédiatement disponible. On observe alors qu'elle existe sous forme phosphorylée : G1P et G6P :
- le fructose (hexose à groupement cétone)
Cette molécule est un D-fructose.
Aussi important que le glucose dans les voies métaboliques, cette molécule se présente sous forme de F1P ou de F1,6bisP :
Les pentoses et les hexoses seulement peuvent se cycliser, forme qu’ils portent à 99% en présence d'eau. Ainsi, les groupements aldéhydes et cétone sont masqués (donc peu réactifs).
Le mécanisme de cyclisation est une réaction intramoléculaire entre deux fonctions de la molécule :
- entre une fonction alcool et la fonction aldéhyde pour un aldose
- entre une fonction alcool et la fonction cétone pour une cétose
La réactivité des oses
[modifier | modifier le wikicode]Les oses cyclisés sont des réducteurs : ils peuvent être oxydés par des sels de métaux lourds en solution alcaline ou par des coenzymes telle le NAD qui devient alors NADH,H⁺
Prenons comme exemple la molécule de glucose cyclisée:
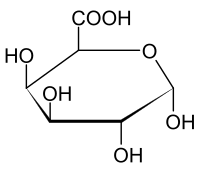
- Cette dernière peut être oxydée en acide glucuronique par transformation, sur le sixième carbone de la chaîne, de la fonction alcool en fonction acide carboxylique :
- Le glucose est également réactif sur le premier carbone de la chaîne :
La fonction alcool du premier carbone peut réagir avec une autre fonction alcool d’une autre molécule (tels des acides aminés comme la sérine ou la thréonine représentés sur la figure par le radical "R") pour réaliser cette liaison.
- Formation de liaison N-glycosidique : dans ce cas, c’est le deuxième carbone de la chaîne qui réagit avec une fonction amine . Cette réaction dite d'amination peut être suivi d’une acétylation : le groupement devient alors:
Les dérivés des oses
[modifier | modifier le wikicode]Le désoxyribose
[modifier | modifier le wikicode]Le désoxyribose est dérivé du ribose, un pentose sous sa forme cyclique. Il a perdu l'oxygène de la fonction alcool du deuxième carbone de sa chaîne. Il est le précurseur des acides nucléiques, constituants de l'ADN.
Les dérivés phosphorylés
[modifier | modifier le wikicode]Les oses en général réagissent beaucoup avec l'acide phosphorique pour former des esters phosphoriques (création de liaison phosphoester). Cela permet de former des molécules plus énergétiques.
Ces éléments sont fondamentaux : ils sont à la base du couplage et du transfert d'énergie notamment dans la glycolyse où le glucose est phosphorylé en glucose-6-phosphate (noté G6P) et portant deux charges négatives :
Molécule de G6P ayant un liaison phosphoester très réactive : 
Ces réactions de phosphorylation sont importantes car elles permettent de séquestrer la molécule (comme ici le glucose par exemple) dans des cellules ou des organites spécifiques. En effet, les membranes sont imperméables aux ions (molécules chargées).
Les dérivés phosphorylés interviennent dans :
- La synthèse du saccharose :
- Bilan réactionnel de la synthèse du saccharose :
- L'élongation de la chaîne du glycogène (par l’intervention de l'UDP-Glucose)
- L'élongation de la chaîne de l'amidon (par l’intervention de l'ADP-Glucose)
- L'élongation de la chaîne de la cellulose (par l’intervention de l'UDP-Glucose)
- La glycosylation des protéines (à partir d'UDP-Galactose)
Les acides uroniques
[modifier | modifier le wikicode]On forme des acides uroniques par oxydation d’un alcool primaire. Ils sont les précurseurs de nombreuses macromolécules dans la matrices extra cellulaire des animaux.
Exemple de l'acide galacturonique et de l'acide glucuronique qui sont, dans l’ordre :
Les osamines
[modifier | modifier le wikicode]- Les osamines sont des oses portant une fonction amine.
- Exemple de la glucosamine et de la galactosamine qui sont, dans l’ordre :
- Il existe également des dérivés acétylés (portant une fonction acétyle) des osamines.
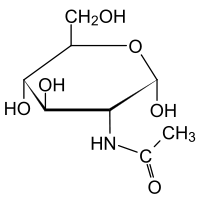
- Exemple de la D-N-acétylglucosamine et de la D-N-acétylgalactosamine:
Pour ceux qui veulent aller plus loin, on peut préciser, par exemple, que la D-N-acétylglucosamine est un précurseur de la chitine qui est un constituant de l'exosquelette des arthropodes…