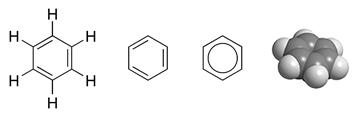
Benzène
Les Arènes
Introduction
Les arènes sont des composés organiques dit aromatiques. En chimie organique les composés aromatiques sont ceux qui comportent un cycle benzénique. On les retrouve dans divers applications : colorants, médicaments, arômes, polymères...
Le benzène
Définition et propriétés physiques
- Formule brute : C6H6
- Température d'ébullition : 80,5 °C
- Température de fusion : 4,4 °C
- Liquide incolore dans des conditions ambiantes
- Masse volumique : 884 kg.m⁻³
- Insoluble dans l'eau
- Toxicologie : l'inhalation répétée,même à très faible dose, de benzène provoque anémie (Benzolisme carence en globule rouge) et cancer. Usage interdit en milieu scolaire. DL50=2g/kg
- Risque chimique : c’est un liquide très inflammable
- Spectre IR : Le benzène et ses dérivés présentent deux bandes intenses vers 700 — 800 cm⁻¹
- Le benzène et ses dérivés ont la particularité d'absorber les rayonnement UV.
Structure
- Représentation de Kékulé (1865)
Kékulé est le premier à imaginer que le benzène soit une molécule cyclique qui comporte une alternance de simple et double liaison. Il envisage que les doubles liaisons peuvent basculer.
- Faits expérimentaux.
| Réactif | Alcène | Benzène |
|---|---|---|
| H2O/H⁺ | CH3-CH=CH2 → CH3-CH(OH)-CH3 | Rien |
| Br2 | CH2=CH2 + Br2 → Br-CH2-CH2-Br |
+ Br2 (seul) → Rien + Br2 (avec UV) → C6H6Br6 (Réaction d’addition) + Br2 (AlCl3) → C6H5Br (Réaction de substitution électrophile aromatique) |
| KMnO4 dilué | → Diol | Rien |
| KMnO4 concentré | → Cétone/acide carboxylique | Rien |
Le benzène ne se comporte pas comme un alcène, il y a des propriétés chimiques plus proches de celles des alcanes.
- Formule réelle
Lors de la formation de la molécule, les orbitales atomiques π se recouvrent toutes pour ne former qu'une seule orbitale moléculaire sur laquelle les 3 paires d'électrons délocalisés vont pouvoir se déplacer.
- La molécule ne possède pas de double liaison : les électrons sont délocalisés.
- La délocalisation stabilise le cycle.